Условие: на фотографиях (Рис. 1а, 1б) представлены два нанобиотехнологических метода визуализации опухоли молочной железы у мышей. В обоих случаях визуализация опухоли осуществляется при облучении животного светом с длиной волны 550-560 нм (а) и 670-690 нм (б), в результате чего опухоль начинает светиться в красной области спектра.
Назовите соединение, которое испускает свет в каждом случае? (1 балл) Назовите метод, при помощи которого был осуществлен синтез этого соединения и укажите место его синтеза в каждом случае (2 балла{увеличено на 1 балл}). Каким образом это соединение ввели в мышь в каждом случае? (1 балл) Каким образом это соединение удалось доставить в опухоль молочной железы и локализовать в ней в каждом случае? (1 балл) Каким образом и с использованием каких методов был смоделирован рак груди на мышах в каждом случае? (2 балла {увеличено на 1 балл}). Можно ли оба представленных метода визуализации опухоли использовать для диагностики опухолевых заболеваний и для каких еще целей можно использовать этот/эти метод(ы)? (1 балл {уменьшено на 1 балл}).
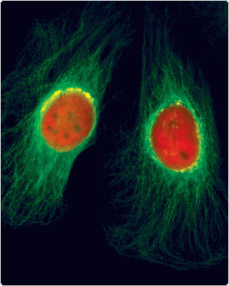
На фотографии (Рис. 2) представлены культивируемые in vitro клетки линии HeLa, которые при облучении их светом с длиной волны 400 нм стали светиться в зеленой, желтой и красной областях спектра.
Какие соединения испускают свет? (1 балл) Назовите структуры (органоиды) клетки, испускающие свет. (1 балл) Назовите биомакромолекулы, «помеченные» различными «цветами» (2 балла {увеличено на 1 балл}). Каким образом удалось различные структуры и биомакромолекулы клетки пометить различными «цветами»? (1 балл) Какие биомакромолекулы ответственны за узнавание различных структур клетки? Каково собирательное название этих биомакромолекул? (1 балл) Какие еще вы знаете биомакромолекулы, способные к специфичному «узнаванию» различных клеток и клеточных структур? (1 балл) Укажите преимущества и недостатки каждой названной вами макромолекулы как молекулы, способной к специфичному «узнаванию» различных клеток и клеточных структур. (2 балла {увеличено на 1 балл})
Ответы:
Назовите соединение, которое испускает свет в каждом случае?
На фотографии слева – красный флуоресцентный белок (максимум поглощения - 557 нм, максимум испускания – 585 нм), на фотографии справа – флуоресцентный краситель Cy5.5 (максимум поглощения - 675 нм, максимум испускания – 694 нм).
Назовите метод, при помощи которого был осуществлен синтез этого соединения и укажите место его синтеза в каждом случае
Синтез красного флуоресцентного белка (RFP) в трансгенных опухолевых клетках человека, имплантированных в мышь, осуществляется так же, как и синтез всех других белков, т.е. посредством процессов транскрипции, трансляции и пострансляционной модификации белка. Место синтеза RFP – клетки рака молочной железы человека линии MDA-MB-435. Синтез флуоресцентного красителя Cy5.5 осуществляется посредством химического синтеза на химическом заводе или в химической лаборатории.
Каким образом это соединение ввели в мышь в каждом случае?
Для того, чтобы ввести RFP мышам, сначала с помощью методов генетической инженерии (конструирование RFP-экспрессирующего вектора, трансфекция опухолевых клеток этим вектором) ввели ген белка в культивируемые клетки рака молочной железы человека линии MDA-MB-435, затем эти клетки, экспрессирующие RFP, имплантировали в жировую ткань мыши, где они сформировали опухоль. Флуоресцентный краситель Cy5.5 ввели мышам в составе наночастиц сложного строения, представляющим собой конъюгат магнитных наночастиц с молекулой Cy5.5 и пептидом EPPT, способным специфически связываться с опухолевым антигеном uMUC-1. При внутривенном введении этой наноконструкции мышам с моделью рака груди, полученной путем имплантации в жировую ткань мыши uMUC-1-позитивных клеток аденокарциномы груди человека линии BT-20, наночастицы специфически аккумулировались в опухоли посредством механизма направленной доставки с помощью лиганда направленной доставки пептида EPPT.
Каким образом и с использованием каких методов был смоделирован рак груди на мышах в каждом случае?
На фотографии слева – рак груди был смоделирован посредством имплантации в жировую ткань трансгенной мыши (с экспрессией в тканях зеленого флуоресцентного белка) клеток рака молочной железы человека линии MDA-MB-435. На фотографии справа – рак груди был смоделирован посредством имплантации в жировую ткань мыши клеток аденокарциномы груди человека линии BT-20.
Можно ли оба представленных метода визуализации опухоли использовать для диагностики опухолевых заболеваний и для каких еще целей можно использовать этот/эти метод(ы)?
Метод визуализации опухоли с помощью RFP нельзя использовать для диагностики опухоли, т.к. RFP экспрессируется только в трансгенных клетках или организмах. Метод визуализации опухоли с помощью введения наночастиц, конъюгированных с флуоресцентными метками и лигандами направленного действия имеет большие перспективы как метода диагностики опухолевых заболеваний, но в клинике пока не используется.
Какие соединения испускают свет?
Квантовые точки Qdot® 525, Qdot® 585 и Qdot® 655 с максимумами излучения, соответственно, 525, 585 и 655 нм.
Назовите структуры (органоиды) клетки, испускающие свет?
Тубулиновые микрофиламенты в цитоплазме (зеленый цвет), структуры аппарата Гольджи (желтый цвет), ядро (красный цвет).
Назовите биомакромолекулы, «помеченные» различными «цветами»
Тубулин (зеленый цвет), гиантин (желтый цвет), нуклеосома (структура, включающая часть двойной цепи ДНК и комплекса белков-гистонов) (красный цвет).
Каким образом удалось различные структуры и биомакромолекулы клетки пометить различными «цветами»?
Благодаря тому, что квантовые точки были конъюгированы со вторичными антителами, которые специфически связывались с предварительно добавленными первичными антителами к соответствующим антигенам. Эти системы представляют собой: 1) крысиные анти–α-тубулин антитела, биотин-конъюгированные козьи анти–крысиные IgG антитела и Qdot® 525 квантовые точки, конъюгированные со стрептавидином (зеленый цвет); 2) кроличьи анти-гиотин антитела и Qdot® 585 квантовые точки, конъюгированные с козьими F(ab’)2 анти–кроличьими IgG антителами (желтый цвет); 3) мышиные анти-нуклеосома антитела и Qdot® 655 квантовые точки, конъюгированные с козьими F(ab’)2 анти–мышиными IgG антителами (красный цвет).
Какие биомакромолекулы ответственны за узнавание различных структур клетки? Каково собирательное название этих биомакромолекул?
Эти биомакромолекулы – моноклональные первичные IgG антителама или иммуноглобулины G типа.
Какие еще вы знаете биомакромолекулы, способные к специфичному «узнаванию» различных клеток и клеточных структур?
Наноантитела, пептиды, лектины, трансферрин и др.
Укажите преимущества и недостатки каждой названной вами макромолекулы как молекулы, способной к специфичному «узнаванию» различных клеток и клеточных структур.
Наноантитела – преимущества: специфическое узнавание, компактность как лигандов для направленной доставки, меньшая иммуногенность; недостатки: очень сложная и дорогая технология получения.
Пептиды – преимущества: компактность как лигандов для направленной доставки, относительная простота получения; недостатки: меньшая по сравнению с антителами селективность, иммуногенность.
Лектины - преимущества: меньшая иммуногенность, высокая специфичность, компактность как лигандов для направленной доставки, относительная простота получения; недостатки: узкая направленность на узнавание полисахаридов.
Трансферрин - преимущества: меньшая иммуногенность, высокая специфичность; недостатки: ограниченность функциональности только в пределах системы Трансферрин–трансфериновый рецептор.
Для более подробного ознакомления:
1. Medarova Z., Rashkovetsky L., Pantazopoulos P., Moore A. Multiparametric monitoring of tumor response to chemotherapy by noninvasive imaging. Cancer Res., 2009, 69(3): 1182-1189;
2. Yang M., Reynoso J., Jiang P., Li L., Moossa A.R., Hoffman R.M. Transgenic nude mouse with ubiquitous green fluorescent protein expression as a host for human tumors. Cancer Res. 2004, 64(23): 8651-8656.