Задача создана по мотивам статьи: Integrated view of genome structure and sequence of a single DNA molecule in a nanofluidic device. / Marie, Rodolphe ; Pedersen, Jonas Nyvold; L. V. Bauer, David ; Rasmussen, Kristian Hagsted; Yusuf, Mohammed; Volpi, Emanuela ; Flyvbjerg, Henrik; Kristensen, Anders; U. Mirb, Kalim.
Proceedings of the National Academy of Sciences of the United States of America, Vol. 110, No. 13, 2013, p. 4893-4898.
- Секвенирование: метод химической деградации, метод обрыва цепи – в обоих случаях образуется набор фрагментов разной длины, с присутствием меченых нуклеотидов на конце. Потом их разделяют с помощью электрофореза. Перед секвенированием необходимо провести амплификацию методом ПЦР. Определяется последовательность нуклеотидов в сегментах до 100-1000 п.н. Метод FISH-гибридизации – определение положения определенных фрагментов ДНК в хромосомах или интерфазных ядрах. Используются флуоресцентно-меченые фрагменты ДНК. Это уже совершенно другой масштаб, уровень целой хромосомы.
- Выделение хромосом из клетки, окрашивание флуоресцентным красителем, разрушение структуры хромосомы (протеолиз), денатурация, ренатурация (ну и позиционирование нити ДНК в нанощели).
- Интеркалирующие красители как правило имеют плоскую гетероциклическую структуру, чтобы встраиваться между азотистыми основаниями. Должны давать интенсивную флуоресценцию, а еще лучше – более интенсивный сигнал в связанном с ДНК виде, чем в свободной форме. Не связываться ковалентно с ДНК, чтобы мог отсоединиться при денатурации, не связываться специфично с определенными участками (необходимо для данного метода), не вызывать изменений длины ДНК при встраивании.
- При термической денатурации ДНК (плавлении) в первую очередь плавятся участки, в которых содержится больше пар АТ, чем ГЦ (т.к. АТ соединяются 2 связями, ГЦ – 3). Т.о. светлые участки – богаты ГЦ парами оснований.
- Разрешение метода в основном будет определяться разрешением флуоресцентного микроскопа, используемого для регистрации карты плавления ДНК, а она в свою очередь определяется длиной волны флуоресценции (или более сложно: 0.6*lambda/NA, где lambda – длина волны света флуоресценции, NA – числовая апертура объектива). Т.е. приблизительно 300 нм. Расстояние между нуклеотидами в цепочке – 0.3 нм (справочные данные), т.о. максимальное разрешение – 1 kb (1 тысяча оснований), это соответствует данным, приведенным в статье. Длина нуклеотидной последовательности, которую можно определить в ячейке – примерно 1.5 Mb (1500000 пар оснований).
- Ренатурация необходима, т.к. в денатурированном виде участки ДНК меняют свою длину.
- Зависимость следующая:
- Проанализированную нить ДНК можно затем амплифицировать и провести как обычное секвенирование, чтобы определить нуклеотидную последовательность, так и использовать в FISH-гибридизации для определения локализации фрагмента в хромосомах.
- Данный метод заполняет пробел между секвенированием, которое может определять последовательность на небольших участках, геномными и клеточными методами исследования ДНК (локализация в хромосомах). Т.о. можно оптимизировать исследования, выбирая для более подробного анализа только интересующие фрагменты больших молекул ДНК. Можно относительно быстро выявлять мутации, имеющие соответствующие размеры (от тысяч до миллионов оснований). Недостатки – такой метод не дает непосредственно нуклеотидной последовательности.
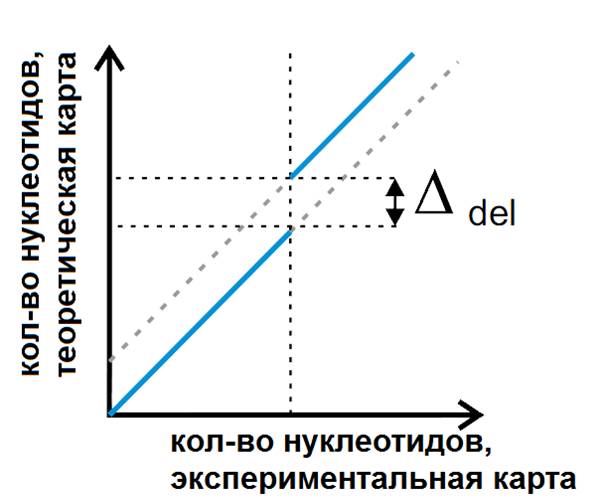
Делеция:
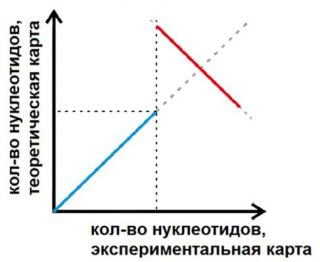
Инверсия:
Важно иметь в виду, что точечные мутации таким образом определить нельзя, только начиная с тысяч п.н.

